结直肠癌(CRC)是一种高度异质性的癌症,探索新的治疗方案是一个迫切需要解决的问题。患者来源的类器官为癌症研究提供了理想的临床前模型,相比于传统的2D培养的肿瘤细胞系,3D培养的类器官可以更好地维持癌症患者的肿瘤特征,其概括了亲代肿瘤组织的分子特征和异质性。最近,许多研究表明,类器官可以精确预测患者对靶向治疗和化疗的反应。一些研究已经利用基于类器官的平台进行抗癌药物筛选,然而,筛选试验主要是基于对细胞生长的测量,而对于抗癌药物的生物学机制和在体内水平上的抗癌机制描述并不多。
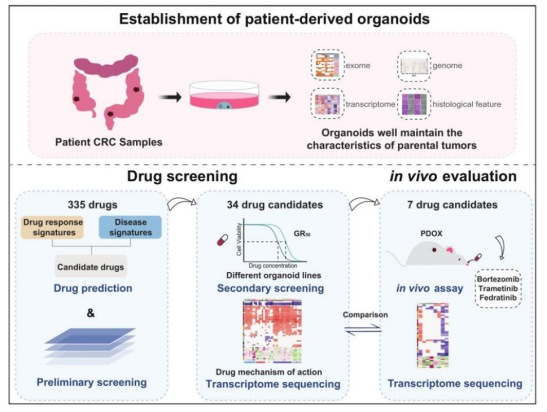
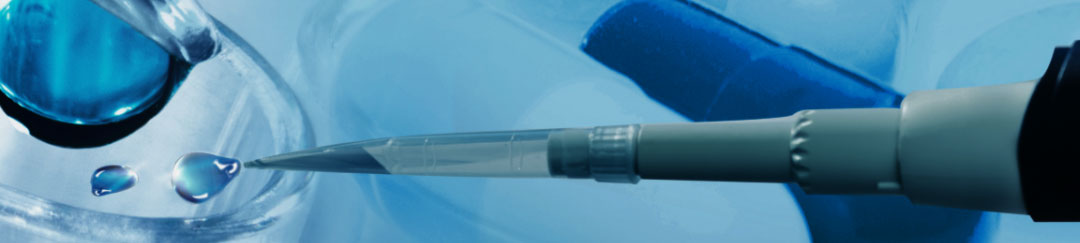
图:总体实验设计方案
2023年6月22日北京大学生物医学前沿创新中心(BIOPIC)汤富酬教授团队与北京大学第三医院普通外科付卫教授团队合作,其中来自北京大学生命科学学院的毛雨诺博士为第一作者,在Protein & Cell期刊发表了一篇名为”Drug repurposing screening and mechanism analysis based on human colorectal cancer organoids“的文章。作者团队开发了一个基于类器官的药物筛选系统,分析了CRC类器官的药物响应特征,并预测了潜在的抗癌药物,以及评估了基于转录组特征的体外和体内药物筛选系统,提供了一种基于测序的药物鉴定策略。

作者首先建立了长期稳定培养的、具有高度代表性的结直肠癌类器官, 观察到患者肿瘤组织的形态各不相同,对应的类器官代表了肿瘤组织的异质性形态。为了进一步表征分子特征,在多组学水平上评估了类器官与亲代肿瘤组织之间的一致性,在类器官和相应的肿瘤组织中发现了CRC中常见突变的关键驱动基因。这些突变根据信号通路或相关基因分为不同类型,如Wnt/β-catenin、RAS/MAPK、PI3K/AKT、TGF、TP53相关通路、JAK/STAT等。结直肠癌的关键驱动基因APC和TP53是结直肠癌中常见的两种突变,在所建立的8个类器官系中均有发现,证明培养的类器官可以很好地概括体内肿瘤的遗传特征。
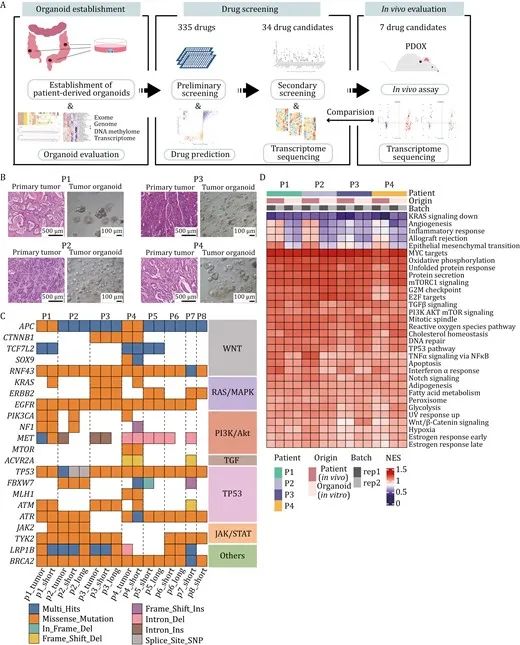
图1:结直肠肿瘤类器官保留了原发组织的组织学结构和基因组特征
该研究基于多个数据库建立了一套药物预测方法,使用经过FDA批准的药物库,并且使用结直肠癌临床常用药5-氟尿嘧啶(5-Fluorouracil)和瑞戈非尼(Regorafenib)作为阳性对照,在包含预测药物的共335种药物中,成功筛选出34种候选药物。为了验证这34种候选药物具有潜在的杀伤结肠癌类器官的能力,该研究在8个结直肠癌类器官系中进行测试,结果发现,不同患者来源的类器官对34种候选药物的敏感性不同,临床上常用的5-氟尿嘧啶和瑞戈非尼两种结直肠癌治疗药物也显示出对不同的类器官系的敏感性不同,说明不同患者之间的药物响应差别大,从侧面反映出类器官筛选药物进而帮助指导患者用药的重要性。
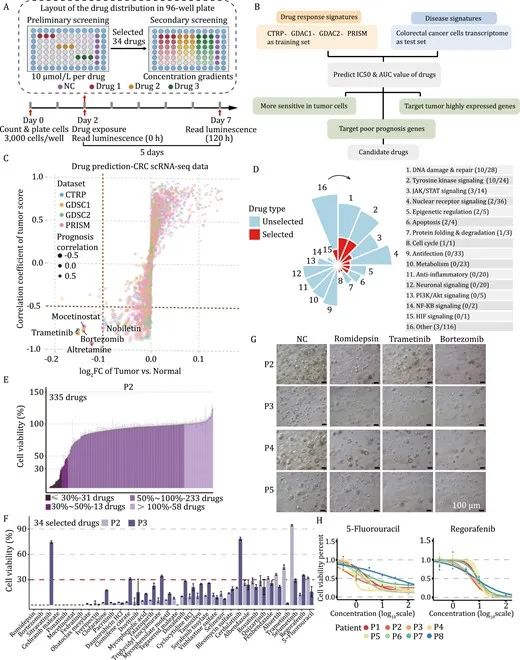
图2:药物预测和基于器官的药物筛选
基于GR50值所代表的药物敏感性,观察到多纳非尼和托磺酸索拉非尼都靶向血管内皮生长因子受体(VEGFR),以及不同类器官系对这两种药物的敏感性表现出高度一致性,不同药物对同一靶点的敏感性在类器官系之间高度一致,表明研究的药物筛选系统的可靠性。比较患者来源的类器官之间的药物敏感性差异,发现不同药物治疗同一类器官系的药物敏感性存在明显差异,同一药物治疗不同类器官系的药物敏感性也存在差异,这表明不同CRC患者之间存在生物学异质性。
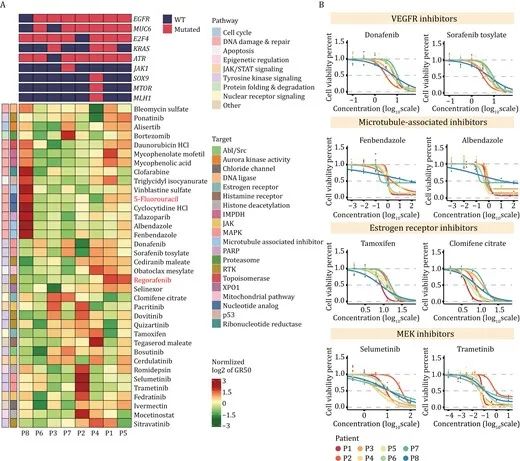
图3:在不同患者来源的类器官中观察到明显的药物敏感性异质性
34种候选药物都对肿瘤类器官有显著的抑制作用,但不同的药物干扰不同的途径,表明它们以不同的方式抑制CRC类器官的活力。根据肿瘤相关信号的表达和基因功能富集分析确定了5种不同的药物反应特征模式。(G1)为分化诱导组,特征是不同肠上皮细胞类型的标记基因表达较高,药物在杀伤肿瘤细胞的同时也可能通过促进细胞分化进而抑制肿瘤细胞的增殖。(G2)为生长抑制组,特征是显著抑制生长因子反应和MAPK信号通路的调节。(G3)为代谢抑制组,特征是其中的化合物抑制结直肠癌类器官代谢相关途径的表达,特别是糖酵解途径。(G4)被注释为免疫反应促进组,特征是其中的化合物抑制肿瘤细胞增殖,而且通过增强肿瘤细胞的抗原呈递特征,促进免疫系统攻击肿瘤细胞。(G5)被确定为细胞周期抑制组,特征是其中的化合物显示细胞周期和DNA复制的下降,其转录组特征表现为有丝分裂纺锤体功能被抑制、铁死亡通路激活,且肠道细胞分化相关基因的表达下调。
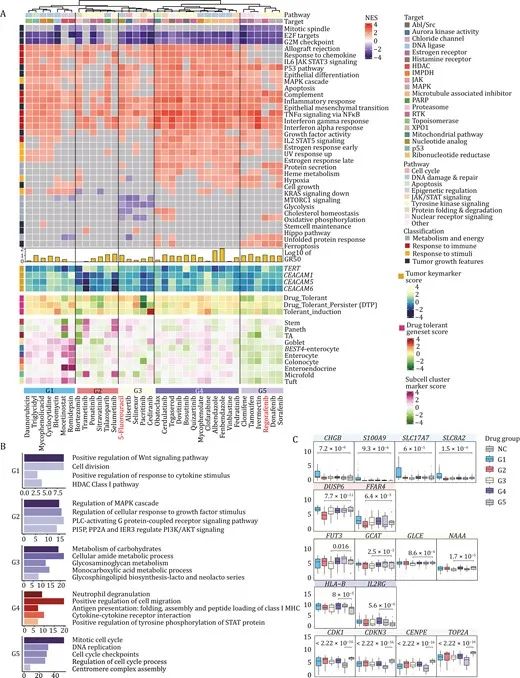
图4:五种不同药物反应模式的转录组特征
通过建立PDOX模型来评估药物在体内环境中的治疗效果。从每个药物反应组(共7种药物)中选择1-2种GR50值较低且临床使用毒性较低的药物进行PDOX抑瘤实验。通过计算药物治疗后小鼠的肿瘤重量,发现筛选的所有药物都有潜在的抑瘤作用,其中,除临床常用药物5-氟尿嘧啶之外,曲美替尼(Trametinib)、硼替佐米(Bortezomib)和菲卓替尼(Fedratinib)的抑制肿瘤的效果明显。根据转录组学数据和蛋白水平结果,进一步验证了曲美替尼、硼替佐米和菲卓替尼可能为治疗结直肠癌的潜在药物。
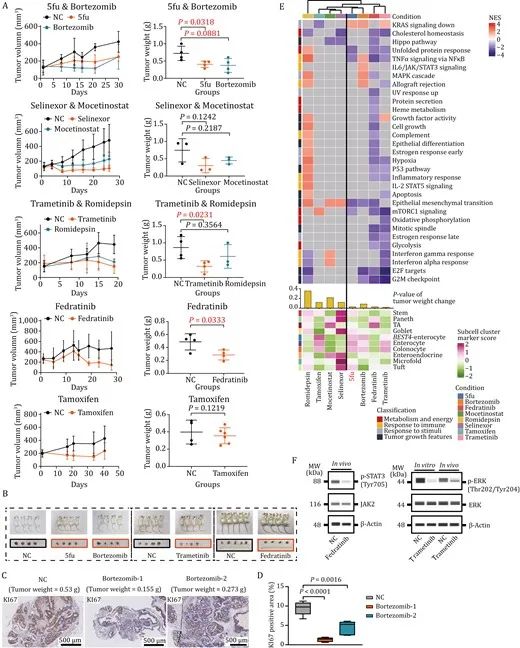
图5:所选药物对PDOX模型的抗癌效果验证
为了排除患者间异质性的影响,该研究进一步比较体外和体内系统(类器官模型和成对PDOX模型)的药物反应差异。在两种系统中,观察到药物处理细胞的转录组变化不一致,其中也包括临床常用药物5-氟尿嘧啶。同时,体外类器官和体内相应的PDOX模型之间只有大约10%的DEG重叠,并且它们之间受干扰途径的表达不同。两种筛选系统之间癌症相关通路的一致性表达在不同的类器官系和不同的药物治疗中也有所不同。
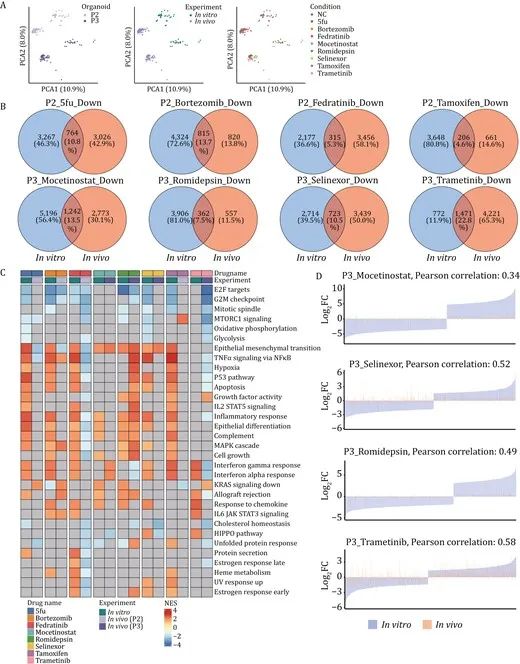
图6:体外培养的类器官与体内建立的PDOX药物转录组特征比较
为进一步研究药物预测方法和基于类器官的药物筛选系统是否可以为CRC的药物联合治疗提供有价值的线索,在具有潜在肿瘤抑制作用的三个药物中,最初被开发用于治疗骨髓纤维的菲卓替尼(Fedratinib)引起了该团队的注意。研究发现,菲卓替尼(Fedratinib)对CRC肿瘤类器官有明显的抑制作用。因此,研究团队利用LINCS数据库来预测可能与菲卓替尼(Fedratinib)有协同作用的药物,其中,硼替佐米(Bortezomib)是排名第一的候选药物。根据两种患者来源的类器官系设置联合用药的梯度浓度,发现联合组的抑瘤效果大于单用药物,说明联用菲卓替尼(Fedratinib)与硼替佐米(Bortezomib)可能具有更大的抑瘤效果,并且在PDOX模型和转录组测序分析中进一步验证了协同效应。

图7:探索类器官作为发现药物联合模型的
可行性
该研究成功建立了基于人类结直肠癌类器官模型的体外药物筛选和药效评价平台,将重组药物库与基于计算的药物预测相结合,共检测335种药物,鉴定出34种具有抗凝血酶作用的药物。候选药物的抗癌活性在已建立的患者源性类器官异种移植(PDOX)体内系统中得到进一步验证。此外,还评估了类器官在体外和PDOX在体内的药物反应特征的一致性和不一致性。根据验证结果,发现菲卓替尼(Fedratinib), 曲美替尼(Trametinib)和硼替佐米(Bortezomib)具有有效的抗癌作用。更重要的是,结合转录组测序,成功揭示了候选药物的作用机制。同时,获得的转录组谱可作为药物研发的宝贵资源。

小鼠结肠类器官培养基套装组分表

人结肠癌类器官培养基套装组分表

肿瘤组织消化液组分表

1. Mao Y, Wang W, Yang J, Zhou X, Lu Y, Gao J, Wang X, Wen L, Fu W, Tang F. Drug repurposing screening and mechanism analysis based on human colorectal cancer organoids. Protein Cell. 2023 Jun 22:pwad038.
2. H. Sung, J. Ferlay, R. L. Siegel, M. Laversanne, I. Soerjomataram, A. Jemal, F. Bray, Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin 71, 209-249 (2021).
3. M. Arnold, M. S. Sierra, M. Laversanne, I. Soerjomataram, A. Jemal, F. Bray, Global patterns and trends in colorectal cancer incidence and mortality. Gut 66, 683-691 (2017).
4. A. Sveen, S. Kopetz, R. A. Lothe, Biomarker-guided therapy for colorectal cancer: strength in complexity. Nat Rev Clin Oncol 17, 11-32 (2020).
5. L. H. Biller, D. Schrag, Diagnosis and Treatment of Metastatic Colorectal Cancer: A Review. JAMA 325, 669-685 (2021).